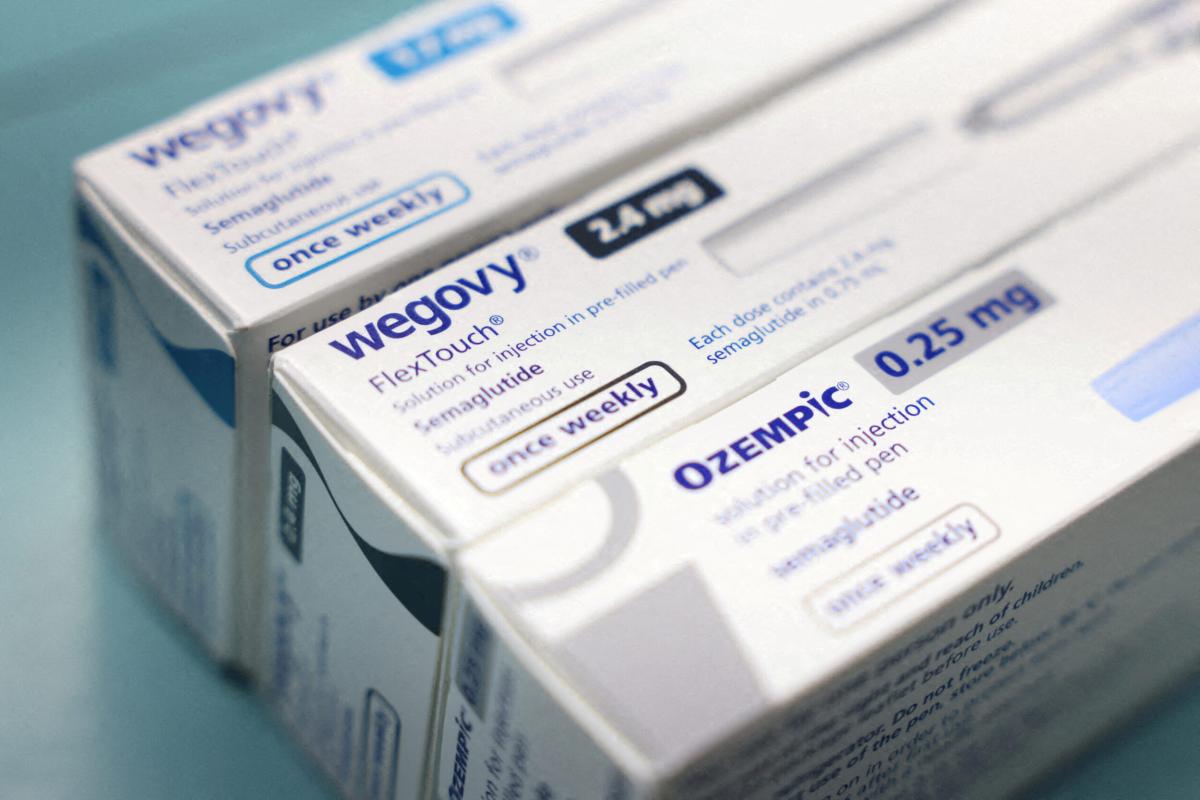
Συναγερμός για Ozempic και Wegovy: Η FDA κατηγορεί την εταιρεία Novo Nordisk ότι «έκρυψε» θανάτους ασθενών
Η νέα παρέμβαση της FDA επαναφέρει στο προσκήνιο ζητήματα φαρμακοεπαγρύπνησης, διαφάνειας και κανονιστικής συμμόρφωσης γύρω από τη Novo Nordisk και τα δημοφιλή σκευάσματά της Ozempic και Wegovy. Η υπόθεση δεν καταλήγει σε συμπέρασμα ότι τα φάρμακα προκάλεσαν τα αναφερόμενα συμβάντα, όμως αναδεικνύει σοβαρές αδυναμίες στον τρόπο με τον οποίο η εταιρεία κατέγραφε και διαβίβαζε αναφορές ανεπιθύμητων ενεργειών προς τις αμερικανικές αρχές.
Η προειδοποιητική επιστολή και τα ευρήματα της FDA
Με προειδοποιητική επιστολή με ημερομηνία 5 Μαρτίου 2026, η Υπηρεσία Τροφίμων και Φαρμάκων των ΗΠΑ (FDA) γνωστοποίησε ότι, ύστερα από έλεγχο που πραγματοποίησε στις εγκαταστάσεις της εταιρείας στο Plainsboro του Νιου Τζέρσεϊ από τις 13 Ιανουαρίου έως τις 7 Φεβρουαρίου 2025, εντόπισε σοβαρές παραβιάσεις των κανόνων για την έγκαιρη αναφορά ανεπιθύμητων ενεργειών μετά την κυκλοφορία φαρμάκων. Στην επιστολή της, η FDA αναφέρει ότι οι πρακτικές της Novo Nordisk «υποδηλώνουν συστημικές αποτυχίες στην παρακολούθηση, καταγραφή, αξιολόγηση και αναφορά» πιθανών ανεπιθύμητων ενεργειών.
Η αμερικανική αρχή επισημαίνει ότι η εταιρεία δεν διαβίβασε εγκαίρως ορισμένα σοβαρά και απρόβλεπτα περιστατικά μέσα στο προβλεπόμενο όριο των 15 ημερών, όπως απαιτεί η ομοσπονδιακή νομοθεσία. Ανάμεσα στα περιστατικά που περιγράφει η επιστολή βρίσκονται τρεις θάνατοι ασθενών που λάμβαναν σεμαγλουτίδη, εκ των οποίων ο ένας αφορούσε αυτοκτονία, καθώς και μία αναφορά για αυτοκτονικό ιδεασμό. Η FDA κατέγραψε επίσης περίπτωση ασθενούς που υπέστη εγκεφαλικό επεισόδιο και έμεινε με αναπηρία ενώ λάμβανε λιραγλουτίδη, χωρίς η αναφορά να σταλεί όπως όφειλε η εταιρεία. Η ίδια η FDA διευκρινίζει ότι δεν υποστηρίζει πως τα φάρμακα προκάλεσαν τα συγκεκριμένα συμβάντα· τονίζει, όμως, ότι η εταιρεία όφειλε να τα αναφέρει ανεξαρτήτως του αν είχε τεκμηριωθεί αιτιώδης σύνδεση.
Οι αδυναμίες στη διαδικασία και η απάντηση της εταιρείας
Σύμφωνα με τα ευρήματα της FDA, η Novo Nordisk σε ορισμένες περιπτώσεις δεν διερεύνησε επαρκώς τις αναφορές, σε άλλες τις απέρριψε χωρίς επαρκή τεκμηρίωση και σε άλλες καθυστέρησε να τις καταγράψει. Η επιστολή περιγράφει ότι η εσωτερική πολιτική της εταιρείας επέτρεπε την απόρριψη περιστατικών όταν ο ασθενής ή ο γιατρός δεν θεωρούσε πως το φάρμακο ευθυνόταν για το συμβάν, παρότι ο νόμος απαιτεί αναφορά ακόμη και όταν η σχέση με το φάρμακο δεν θεωρείται σαφής. Η FDA στάθηκε επίσης στον τρόπο λειτουργίας των τηλεφωνικών κέντρων και στην πρακτική απόρριψης φακέλων όταν δεν υπήρχε συγκατάθεση για περαιτέρω επικοινωνία, κρίνοντας ότι τέτοιες επιλογές δεν συνάδουν με το κανονιστικό πλαίσιο.
Η εταιρεία απάντησε ότι εργάζεται ήδη για να διορθώσει τα προβλήματα που εντόπισε ο έλεγχος και υποστήριξε πως η επιστολή αφορά κυρίως θέματα συμμόρφωσης και «δεν καταλήγει σε συμπεράσματα για την ποιότητα ή την ασφάλεια των φαρμάκων». Παράλληλα, επανέλαβε ότι οι αναφορές ανεπιθύμητων ενεργειών από μόνες τους δεν αποδεικνύουν ότι ένα φάρμακο προκάλεσε ένα περιστατικό. Η εκπρόσωπος της εταιρείας, Λιζ Σκρμπκόβα, δήλωσε ότι «η ασφάλεια και η αποτελεσματικότητα των φαρμάκων GLP-1 διασφαλίζονται όταν χρησιμοποιούνται σωστά και υπό ιατρική παρακολούθηση».
Νομικές κινήσεις και νέο κύμα ανησυχίας
Η υπόθεση αποκτά μεγαλύτερο βάρος επειδή έρχεται σε μια περίοδο κατά την οποία η χρήση των GLP-1 φαρμάκων έχει εκτοξευθεί στις ΗΠΑ. Έρευνες και αναλύσεις έχουν δείξει ότι περίπου 12% των Αμερικανών ενηλίκων έχουν χρησιμοποιήσει τέτοιου τύπου φάρμακα, γεγονός που εξηγεί γιατί κάθε νέα ρυθμιστική παρέμβαση προκαλεί τόσο έντονο ενδιαφέρον. Την ίδια στιγμή, αυξάνονται και οι νομικές διεκδικήσεις από ασθενείς που υποστηρίζουν ότι οι εταιρείες δεν ανέδειξαν επαρκώς πιθανούς κινδύνους, ενώ η Novo Nordisk και η Eli Lilly απορρίπτουν τις κατηγορίες και δηλώνουν ότι θα υπερασπιστούν την ασφάλεια των προϊόντων τους.
Αξίζει ακόμη να σημειωθεί ότι αυτή δεν αποτελεί τη μοναδική πρόσφατη τριβή της Novo Nordisk με τη FDA. Στις αρχές του 2026, η αμερικανική αρχή είχε ήδη απευθύνει νέες επισημάνσεις προς την εταιρεία και για παραπλανητική διαφημιστική προβολή του Ozempic, ενώ είχε προηγηθεί και άλλη παρέμβαση για το Wegovy. Μέσα σε αυτό το πλαίσιο, η τελευταία επιστολή δεν λειτουργεί ως μεμονωμένο επεισόδιο, αλλά ως ακόμη ένα στοιχείο αυξημένης εποπτείας γύρω από έναν από τους ισχυρότερους παίκτες της φαρμακευτικής αγοράς.
Πηγή
Διαβάστε επίσης:
-
Ραγδαίες πολιτικές εξελίξεις: Παραιτούνται 2 από την Κυβέρνηση λόγω ΟΠΕΚΕΠΕ, ηχηρές αποχωρήσεις
-
Γεννήθηκαν με το.. χάρισμα: Αυτά είναι τα 4 ζώδια με το πιο ισχυρό ένστικτο, δεν πέφτουν «έξω» ποτέ
-
Ανακοινώνει χαράτσι: Η απόφαση του Κυριάκου Μητσοτάκη που προκαλεί σεισμό στην αγορά